Hekzakloroetan
 | |
 | |
| Adlandırmalar | |
|---|---|
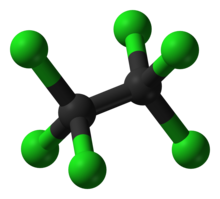
Tercih edilen IUPAC adı Hexachloroethane | |
Diğer adlar Karbon hekzaklorür, etan hekzaklorür, Perkloroetan | |
| Tanımlayıcılar | |
| |
3D model (JSmol) |
|
| 1740341 | |
| ChEBI |
|
| ChEMBL |
|
| ChemSpider |
|
| ECHA InfoCard | 100.000.606 |
| EC Numarası |
|
| 26648 | |
| KEGG |
|
PubChem CID |
|
| UNII |
|
CompTox Bilgi Panosu (EPA) |
|
InChI
| |
SMILES
| |
| Özellikler | |
| Molekül formülü | C2Cl6 |
| Molekül kütlesi | 236.74 g/mol |
| Görünüm | renksiz kristal katı[1] |
| Koku | kâfur benzeri[1] |
| Yoğunluk | 2.091 g/mL at 25 °C |
| Erime noktası | sublimes |
| Kaynama noktası | 183 ila 185 °C (361 ila 365 °F; 456 ila 458 K) |
| Çözünürlük (su içinde) | %0,005(22.2 °C)[1] |
| Buhar basıncı | 0.2 mmHg (20 °C)[1] |
| -112.7·10−6 cm3/mol | |
| Tehlikeler | |
| İş sağlığı ve güvenliği (OHS/OSH): | |
| Ana tehlikeler | Olası kanserojen, kuvvetli MSS depresanı |
| NFPA 704 (yangın karosu) |  2 0 0 |
| Parlama noktası | noncombustible[1] |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz) | 4460 mg/kg (sıçan, oral) 4970 mg/kg (gine domuzu, oral) |
| NIOSH ABD maruz kalma limitleri: | |
| PEL (izin verilen) | TWA 1 ppm (10 mg/m3) [cilt][1] |
| REL (tavsiye edilen) | Ca TWA 1 ppm (10 mg/m3) [cilt][1] |
| IDLH (anında tehlike) | Ca [300 ppm][1] |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
| Bilgi kutusu kaynakları | |
Hekzakloroetan (perkloroetan olarak da bilinir), hidrojenlerinin tamamı klorla yer değiştirmiş bir etan türevidir. C2Cl6 formülüne sahip, süblimleşme eğilimi gösteren beyaz bir katıdır.
Kullanımları
Aşırı basınç yağlayıcılarının formülasyonunda hekzakloroetan kullanılmıştır. Propilen tetrafloroetilen kopolimerinin emülsiyon polimerizasyonunda bir zincir transfer maddesi olarak da kullanılmıştır. Hekzakloroetan, veterinerlik tıbbında antihelmintik, kauçuk hızlandırıcı, fungisidal ve insektisidal formülasyonların bir bileşeni ve ayrıca bir güve kovucu ve selüloz esterleri için bir plastikleştirici olarak kullanılmıştır.[3]
Sis bombaları
Hekzakloroetan dumanı veya HC dumanı olarak adlandırılan sis bombaları, kabaca eşit miktarda hekzakloroetan ve çinko oksit ve yaklaşık %6 granüler alüminyum içeren bir karışım kullanır. Bu dumanlar zehirlidir ve çinko klorür (ZnCl2) içerir.[4][5] Steinritz ve arkadaşlarına göre, "Potansiyel akciğer toksisitesi nedeniyle" çinko klorür üreten sis bombaları "çoğu batı ülkesinin cephaneliğinden çıkarılmıştır."[6]
Üretim
Tetrakloroetilenin 100–140 °C'de ferrik klorür varlığında klorlanması en yaygın kullanılan ticari üretim yöntemidir, ancak birkaç başka yöntem de mevcuttur. Klor ile baryum karbürü reaksiyona sokarak küçük ölçekte yüksek saflıkta bir form üretilebilir.[7] Endüstriyel klorlama işleminin ürünüdür.
Tehlikeleri
Hekzakloroetan ağızdan alındığında karaciğere zarar verir ve yüksek konsantrasyonlarda solunduğunda hafif bir narkotik etkiye sahiptir. Ne kadar kanserojen olabileceği uzun zamandır araştırılmaktadır. Suda çözünmediği için katı hâlde tehlikeli değildir. Oda sıcaklığında yavaş yavaş süblimleşir.
Kaynakça
 | Organik kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |
- ^ a b c d e f g h NIOSH Pocket Guide to Chemical Hazards. "#0316". National Institute for Occupational Safety and Health (NIOSH).
- ^ "Hexachloroethane". Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Sağlığı ve Güvenliği Enstitüsü (NIOSH). Arşivlenmesi gereken bağlantıya sahip kaynak şablonu içeren maddeler (link)
- ^ Snedecor, Gayle (1999). "Hexachloroethane". In Kroschwitz, Jacqueline I. (ed.). Kirk-Othmer Concise Encyclopedia of Chemical Technology
- ^ "Appendix E: Smoke And Masking Agents" (PDF). Australian Department of Veteran Affairs. December 2003. s. E-3. 13 Şubat 2014 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 4 Ekim 2012.
- ^ National Research Council (1997). Toxicity of Military Smokes and Obscurants, volume 1. Subcommittee on Military Smokes and Obscurants. Washington, DC: National Academy Press. p. 127
- ^ Steinritz, D., Zehfuß, F., Stenger, B., Schmidt, A., Popp, T., Kehe, K., Mückter, H., Thiermann, H., Gudermann, T. (2018). Zinc chloride-induced TRPA1 activation does not contribute to toxicity in vitro. Toxicology Letters, 293, 133–139. doi:10.1016/j.toxlet.2017.09.008
- ^ "Hexachloroethane 101" (PDF). September 1997. 29 Mayıs 2003 tarihinde kaynağından (PDF) arşivlendi.











