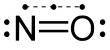Azot monoksit
 | |||
| |||
| Adlandırmalar | |||
|---|---|---|---|
Azot monoksit | |||
Sistematik IUPAC adı Oksidonitrojen(•)[1] (ilave) | |||
Diğer adlar Nitrik oksit Azot(II) oksit | |||
| Tanımlayıcılar | |||
| |||
3D model (JSmol) |
| ||
| 3DMet |
| ||
| ChEBI |
| ||
| ChEMBL |
| ||
| ChemSpider |
| ||
| DrugBank |
| ||
| ECHA InfoCard | 100.030.233 | ||
| EC Numarası |
| ||
| 451 | |||
IUPHAR/BPS |
| ||
| KEGG |
| ||
PubChem CID |
| ||
| RTECS numarası |
| ||
| UNII |
| ||
| UN numarası | 1660 | ||
CompTox Bilgi Panosu (EPA) |
| ||
InChI
| |||
SMILES
| |||
| Özellikler | |||
| Kimyasal formül | NO | ||
| Molekül kütlesi | 30,01 g mol−1 | ||
| Görünüm | Renksiz gaz | ||
| Yoğunluk | 1.3402 g/L | ||
| Erime noktası | −164 °C | ||
| Kaynama noktası | −152 °C | ||
| Çözünürlük (su içinde) | 0.0098 g / 100 ml (0 °C) 0.0056 g / 100 ml (20 °C) | ||
| Kırınım dizimi (nD) | 1.0002697 | ||
| Yapı | |||
| doğrusal (nokta grubu C∞v) | |||
| Termokimya | |||
Standart molar entropi (S⦵298) | 210.76 J/(K•mol) | ||
Standart formasyon entalpisi (ΔfH⦵298) | 91.29 kJ/mol | ||
| Farmakoloji | |||
| soluma | |||
| Farmakokinetik: | |||
| iyi | |||
| pulmoner kapiller yoluyla | |||
| 2–6 saniye | |||
| Tehlikeler | |||
| GHS etiketleme sistemi: | |||
| Piktogramlar |     | ||
| R-ibareleri | R8, R23, R34, R44 | ||
| G-ibareleri | S1, S17, S23, S36/37/39, S45 | ||
| Tehlike ifadeleri | H270, H280, H314, H330 | ||
| Önlem ifadeleri | P220, P244, P260, P280, P303+P361+P353, P304+P340, P305+P351+P338, P315, P370+P376, P403, P405 | ||
| NFPA 704 (yangın karosu) |  3 0 3 OX | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LC50 (medyan konsantrasyon) | 315 ppm (tavşan, 15 dak.) 854 ppm (sıçan, 4 saat) 2500 ppm (fare, 12 dak.)[2] | ||
LCLo (yayınlanan en düşük) | 320 ppm (fare)[2] | ||
| Güvenlik bilgi formu (SDS) | Dış MSDS | ||
| Benzeyen bileşikler | |||
| Azot pentaoksit Azot tetraoksit Diazot trioksit Azot dioksit Nitröz oksit Nitroksil (indirgenmiş formu) Hidroksilamin (hidrojenlenmiş formu) | |||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
| Bilgi kutusu kaynakları | |||
Azot monoksit, kimyasal formülü NO olan bir bileşiktir. Bu gaz, -insanlar da dahil olmak üzere- memelilerin vücutlarında önemli bir sinyal molekülü olmasının yanı sıra kimyasal endüstride de önemli bir ara üründür. Ayrıca NO, araba motorları ve elektrik santralleri tarafından üretilerek hava kirliliğine neden olur.
NO, memeli vücudundaki yararlı veya zararlı birçok fizyolojik ve patolojik süreçte rol oynayan önemli bir sinyal molekülüdür.[3] Uygun dozlarda NO üretimi, birçok organın zarar görmesinin engellenmesinde (karaciğerin iskemik hasardan korunması gibi) önemlidir. Ancak yüksek dozlarda NO, doğrudan doku zehirlenmesine yol açtığı gibi, septik şokla tetiklenen dolaşım sistemi çöküşüne de katkıda bulunur. Ayrıca kronik NO salınımı, Tip I juvenil diyabet, multiple skleroz, artrit, ülseratif kolit gibi birçok iltihabi hastalık ve kanser türüyle ilişkilendirilmiştir.[4]
Azot monoksit, kimyasal formülü N2O olan bir genel anestetik madde olan Nitröz Oksit ile ya da bir başka hava kirletici madde olan Azot Dioksit (NO2) ile karıştırılmamalıdır. Azot monoksitin kimyasal etkinliğinin oldukça yüksek olması, bir serbest radikal olduğunun anlaşılmasına uygundur. Havadaki Ozon ile tepkimeye girerek NO2 oluşmasını sağlar. Bu reaksiyon, ortaya çıkan kırmızı-kahverengi renk ile kolaylıkla tanınabilir.
Basit bir molekül olmasına rağmen, NO, sinir sistemi, fizyoloji, immunoloji gibi alanlarda yapılan birçok araştırmanın temel molekülüdür. Ayrıca NO, 1992 yılında AAAS (American Association for the Advancement of Science, Amerikan Bilim Gelişimi Kuruluşu) tarafından Yılın Molekülü seçilmiştir.[5]
Kimyasal özellikleri
Termodinamik açıdan bakıldığında, NO O2 ve N2 bileşiklerinden daha kararsızdır, bu çevrim katalist bir madde olmadığı sürece çok yavaştır. NO oluşumu endotermik bir olaydır, 1000 °C üstü sıcaklıklarda mümkün olmaktadır. Şimşek NO oluşumunun doğal bir kaynağıdır.İçten yanmalı motor kullanan taşıtların yaygınlaşması çevrede NO düzeylerini hatırı sayılır derecede artırmıştır. Arabalarda bulunan katalitik dönüştürücülerin bir amacı da oluşan NO'yu O2 ve N2'ye geri çevirerek çevreye yayılan NO miktarını azaltmaktır.
Havadaki azot monoksit nitrik aside dönüşebilir, ki bu da asit yağmurunda görülür. Ek olarak, hem NO hem de NO2 ozon tabakası silinmesinde pay sahibidirler. Azot monoksit ufak,yüksek oranda difüzyona uğrayan bir gazdır ve önemli bir biyoaktif moleküldür.
Etki mekanizması
Canlı hücrelerde NO için birçok etki mekanizması gösterilmiştir. Bunlar; ribonükleotid redüktaz ve akonitaz gibi demirli proteinlerin oksidasyonu,guanilat siklaz aktivasyonu ve buna bağlı etkiler,proteinlere yapılan ADP ribozilasyonu,proteinlerin sülfhidril gruplarının nitrozilasyonu ve demir metabolizmasının düzenlenmesidir.[6] NO'nun kanın mononükleer akyuvarlarında iNOS gen ekspresyonu ve iltihabi yanıttan sorumlu önemli bir transkripsiyon faktörü olan NFkB aktivasyonu yaptığı gösterilmiştir.[7] NO'nun siklik GMP sentezinden sorumlu sitozolik heterodimerik bir enzim olan guanilat siklaz aktivasyonu yaptığı gösterilmiştir. Siklik GMP'nin bazı protein kinazları aktive ederek miyozin hafif zincirinin defosforilasyonuna yol açtığı bilinmektedir. Bu da düz kas gevşemesi anlamına gelmektedir (özellikle damar düz kası gevşemesi ve vazodilatasyon).[8]
Teknik uygulamaları
NO'nun doğrudan kullanımı olmamasına rağmen amonyaktan nitrik asit sentezinin yapıldığı Ostwald sürecinde üretilen bir ara üründür.2005'te yalnızca ABD'de 6 milyon ton nitrik asit üretimi gerçekleştirilmiştir.[9] Ayrıca yarı iletken endüstrisinde de pay sahibi olmuştur.CMOS aygıtlarda nitröz oksit ile birlikte oksinitrit kapılarını oluşturmak için yararlanılmaktadır.
Diğer kullanımları
Azot monoksit polimerlerdeki yüzey radikallerini saptamada kullanılabilir.Yüzey radikallerini NO ile ortadan kaldırmak azot inkorporasyonu ile sonuçlanır ki bu değer X-ray fotoelektron spesktroskopi tekniğiyle ölçülebilir.
Biyolojik işlevleri
NO sinyal iletiminde görevli bilinen birkaç gazdan birisidir.Omurgalılarda anahtar role sahip bir sinyal molekülüdür ve birçok biyolojik süreçte rol oynamaktadır.Önceleri Endotel-kaynaklı gevşetici faktör(EKGF,EDRF)olarak bilinen bu molekül çok sayıda nitrik oksit sentaz(NOS) enzimlerinin yardımıyla arjinin ve oksijenden veya inorganik nitrat gruplarının indirgenmesiyle nitrovazodilatör ilaç moleküllerinden sentezlenmektedir. Damarın içteki endotel tabakası NO sinyaliyle kendisini kuşatan damar düz kasını gevşetir bu da vazodilatasyon ve artmış kan akımı ile sonuçlanır. Azot monoksit çok reaktif bir bileşiktir (birkaç saniyelik yarıömrü vardır) ve membranlardan hızlıca difüzyona uğramaktadır. Bu da belki de onun ideal bir sinyal molekülü olmasını açıklayan görüştür.[10] Yüksek rakımlı yerlerde yaşayan insanlarda hipoksi oluşumunu önlemek için NO sentezi artar. NO'nun vazodilatasyonun yanı sıra bir nörotransmitter olduğu (bakınız Gazotransmitterler) ayrıca saç ve kıl oluşumunda rolü olduğu(bakınız Minoksidil ve penil ereksiyonda da vazgeçilmez bir rolü olduğu bilinmektedir.Nitrogliserin ve amil nitrit NO açığa çıkardığı için vazodilatör ilaç olarak kullanılmaktadır.Sildenafil, popüler olarak bilinen adıyla Viagra NO sinyal yolunun sürekliliğini sağlayarak penisin ereksiyon halini korur.
Azot monoksit (NO) damar düz kasının kasılmasını ve büyümesini,kan pulcuğu kümelenmesini ve endotele akyuvar yapışmasını inhibe ederek damar homeostasisinde olmazsa olmaz bir yer edinmektedir.İnsanlarda besinlerle aşırı tuz alımının NO salınımını bozduğu gösterilmişir.[11]
Azot monoksit ayrıca insanda immun yanıtın bir bileşeni olarak makrofaj ve nötrofillerde de üretilmektedir.Bakteri ve insanda patojen olan diğer organizmalara karşı toksik etki göstermektedir. Ama günümüzde birçok bakteri No'ya karşı direnç mekanizmaları geliştirmiştir.[12] Azot monoksitin ayrıca havayolunun astım gibi iltihabi hastalıklarında iltihabın düzeyinin göstergesi olduğunun düşünülmesi, bir nefes testi olarak ekshale edilen NO ölçümünün gündeme gelmesini sağlamıştır.
Azot monoksit aynı zamanda süperoksitlerle tepkimeye girerek peroksinitrit oluşturduğu için iskemi sonrası gelişen reperfüzyon hasarı sürecine katkıda bulunabilir. Çelişircesine, parakuat zehirlenmesinde solunan NO'nun yararlı olduğu bilinmektedir.
Bitkilerde, 4 ayrı yoldan biriyle sentezlenmektedir:(i)L-arjinin-bağımlı azot oksit sentaz,[13][14][15] (her ne kadar bitkilerde hayvan NOS analogu enzimler olduğu tartışmalı olsa da),[16] (ii) plazma membranına bağlı nitrat redüktaz, (iii) mitokondrial ETS ile, ya da (iv) enzimatik olmayan tepkimelerle. Bitkilerde de bir sinyal molekülüdür, esas olarak oksidatif strese karşı görev yapar ve bitkilerin patojenlerle başa çıkmasını sağlar. Viagra ile muamele edilen koparılmış çiçeklerin solmadan önce daha uzun süre dayandığı ve dik durduğu gösterilmiştir.[17]
Azot monoksitin biyolojik öneme sahip bir diğer tepkimesi de S-nitrozilasyon tepkimesidir, bu işlemle tiyoll grupları, örneğin proteinlerdeki sistein kalıntıları,S-nitrozotiyolleri (RSNOlar) verirler. S-Nitrozilasyon birçok önemli protein için bir posttranslasyonel düzenleme mekanizmasıdır.
Pediatrik Yoğun Bakımda Kullanımı
Nitrik Oksit/Oksijen karışımları yenidoğanlarda primer pulmoner hipertansiyonun ve tedavisinde kapiller ve pulmoner dilatasyon sağlamak için ve post mekonyum aspirasyonda kullanılmaktadır,ayrıca doğum lekeleriylen ilişkilendirilmiştir.[18][19] Bunlar ECMO kullanımından önce son-çare gaz karışımlarıdır.NO tedavisi pulmoner vasküler hastalıkları olan yenidoğanlarda hayatı kurtarabilmektedir.[20]
Tepkimeleri
- Oksijene maruz kaldığında, NO azot diokside dönüşür.
- 2NO + O2 → 2NO2
- Bu birleşmenin ONOONO denen bir ara ürün aracılığıyla olduğu düşünülmektedir. Suda, NO oksijen ve suyla tepkimeye girerek HNO2 ya da nitröz asit verir. Bu tepkime şöyle olmaktadır:
- 4 NO + O2 + 2 H2O → 4 HNO2
- NO flor, klor ve brom ile de tepkime verir,XNO bileşiklerini oluşturur, bunlar nitrozil halidler olarak bilinirler(örneğin nitrozil klorür) İyotla da tepkimeye girebilir ve Nitrozil iyodür de oluşur ama çok kısa bir süre içinde eski haline döner.
- 2NO + Cl2 → 2NOCl
- Nitroksil (HNO) nitrik oksidin indirgenmiş biçimidir.
- Azot oksit aseton ve alkoksid ile tepkimeye girerek diazeniumdiolat ya da nitrozohidroksilamin ve Metil asetat verir. ]::[21]

- Bu Traube tepkimesi olarak bilinen eski bir tepkimedir (1898) ama NO ön ilaç araştırması dolayısıyla yeniden gündeme gelmiştir.Sodyum metoksit ile de tepkimeye girerek Sodyum format ve nitröz oksit verir.[22]
Hazırlanması
- Yukarıda belirtildiği gibi, nitrik oksit yüksek sıcaklıklarda endüstriyel olarak doğrudan O2 ve N2'den üretilmektedir.Laboratuarda ise nitrik asidin indirgenmesiyle hzırlanmaktadır.
- 8HNO3 + 3Cu → 3Cu(NO3)2 + 4H2O + 2NO
- ya da nitröz asidin indirgenmesiyle
- 2 NaNO2 + 2 NaI + 2 H2SO4 → I2 + 4 NaHSO4 + 2 NO
- 2 NaNO2 + 2 FeSO4 + 3 H2SO4 → Fe2(SO4)3 + 2 NaHSO4 + 2 H2O + 2 NO
- 3 KNO2(l) + KNO3 (l) + Cr2O3(s) → 2 K2CrO4(s) + 4 NO (g)
- Demir(II) sülfat yolu basit olup üniversite öğrencilerine deney amaçlı olarak gösterilmektedir.
- Ticari olarak, NO amonyağın 750 °C ila 900 °C (normali 850 °C) katalist olarak platin varlığında oksitlenmesiyle elde edilir:
- 4NH3 + 5O2 → 4NO + 6H2O
- Endotermik O2 ve N2 tepkimesi (>2000 °C) sıcaklıklarda şimşek çakarken kendiliğinden gelişmektedir.
- N2 + O2 → 2NO
Koordinasyon Kimyası
NO tüm geçiş metalleriyle metal nitrozilleri denen kompleksler vermektedir.NO'nun en yaygın bağlanma biçimi terminal linear tiptir (M-NO).M-N-O grubunun açısı 160-180° arasında değişebilmektedir ama yie de doğrusal olarak anılmaktadır.NO grubu tek bir elektron vericisi olarak göze çarpmaktadır.[23] Buna benzer kompleksler CO ile izoelektronik olan NO+ tepkimelerinde de gözlenmektedir.
Azot monoksit bir tek elektron psödohalidi olarak iş görebilir. Bu durumda M-N-O grubu açısı 120-140° civarında olmaktadır.
NO grubu ayrıca birçok moleküler geometride azot atomu aracılığıyla metal merkezleri arasında köprüler kurabilir.
NO derişiminin ölçülmesi
NO derişimi ozon içeren basit bir kemiluminesan tepkimeyle ölçülebilir.[24] NO içeren bir örnek bol miktarda ozon içeren bir yere konur. Azot monoksit ozonla tepkimeye girerek oksijen ve azot dioksit verir. Bu tepkime ayrıca bir fotodetektör yardımıyla saptanabilir. üretilen ışık miktarı NO miktarıyla doğru orantılıdır.
- NO + O3 → NO2 + O2 + ışık
Diğer bir test yöntemi olan elektroanaliz(amperometrik yaklaşım) sırasında NO voltaj değişimi oluşturan bir elektrod gibi davranır.NO'nun in vivo ortamda ölçümü kısa yarıömrü dolayısıyla çok daha zordur. Birkaç yararlı yöntemden birisi azot oksidin demir-ditiyokarbamat radikalleriyle tuzaklandığı dönüş tuzağı (spin trapping) yöntemidir. Oluşan mononitrozildemir EPR(Elektron Paramanyetik Rezonans) ile ölçülür.[25][26]
Hücreiçi ölçümler için asetillenmiş formda fluoresan boya türleri kullanılmaktadır.Oluşan ürün DAF-2(4,5-diaminofluoreskan)[27]
Besin desteği
Azot monoksit vücut geliştiriciler için bir besin desteği olarak alınabilir.GNC vücut geliştiriciler için oral NO tabletleri hazırlamakta ve kas gelişiminde çok önemli olduğunu öne sürmektedir fakat bu klinik denemelerle doğrulanmış değildir.
Kaynakça
- ^ "Nitric Oxide (CHEBI:16480)". Chemical Entities of Biological Interest (ChEBI). Birleşik Krallık: European Bioinformatics Institute. 11 Mayıs 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 27 Haziran 2020.
- ^ a b "Nitrik oksit". Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Sağlığı ve Güvenliği Enstitüsü (NIOSH). Arşivlenmesi gereken bağlantıya sahip kaynak şablonu içeren maddeler (link)
- ^ Hou Y.C., Janczuk A. and Wang P.G. (1999): Current trends in the development of nitric oxide donors. Curr. Pharm. Des. June, 5 (6): 417- 471
- ^ Tylor B.S., Kion Y.M., Wang Q.I., Sharpio R.A., Billiar T.R. and Geller D.A. (1997): Nitric oxide down regulates hepatocyte-inducible nitric oxide synthase gene expression. Arch. Surg. 1, (32). Nov.; 1177-1182.
- ^ Elizabeth Culotta and Daniel E. Koshland Jr (Aralık 1992). "NO news is good news. (nitric oxide; includes information about other significant advances & discoveries of 1992) (Molecule of the Year)". Science. 258 (5090). ss. 1862-1864. doi:10.1126/science.1361684. PMID 1361684.
- ^ Shami P.J., Moore J.O., Cockerman J.P., Halhorn W.J., Misukonis M.A., and Weinberg J.B. (1995): Yeni izole edilmiş non-lenfositik lösemi hücrelerinde büyüme ve farklılaşmanın NO tarafından düzenlenmesi. Leukaemia Research; 19(8): 527 - 534.
- ^ Kaibori M., Sakitani K., Oda M., Kamiyama Y., Masu Y. and Okumura T.(1999). Immunosuppressant FK56 inhibits iNOS gene expression at a step of NK-Kappa B activation in rat hepatocytes. J. Hepatol. Jan; 30 (6): 1138-1145.
- ^ Denninger J.W. and Marletta M.A. (1999): Guanylate cyclase and the No/cGMP singling pathway. Biochem. Biophys. Acta, May; 1411 (2-3): 334-356.
- ^ “Production: Growth is the Norm” Chemical and Engineering News, July 1 0, 2006, p. 59.
- ^ Stryer, Lubert (1995). Biochemistry, 4th Edition. W.H. Freeman and Company. ss. pp. 732. ISBN 0-7167-2009-4. KB1 bakım: Fazladan yazı (link)
- ^ "Arşivlenmiş kopya". 11 Aralık 2010 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Ağustos 2008.
- ^ C. A. Janeway; ve diğerleri. (2005). Immunobiology: the immune system in health and disease (6. ed. bas.). New York: Garland Science. ISBN 0-8153-4101-6. KB1 bakım: Diğerlerinin yanlış kullanımı (link) KB1 bakım: Fazladan yazı (link)
- ^ Corpas; ve diğerleri. (2004). "Cellular and subcellular localization of endogenous nitric oxide in young and senescent pea plants". Plant Physiology. 136 (1). ss. 2722-33. doi:10.1104/pp.104.042812. PMID 15347796. KB1 bakım: Diğerlerinin yanlış kullanımı (link)
- ^ Corpas; ve diğerleri. (2006). "Constitutive arginine-dependent nitric oxide synthase activity in different organs of pea seedlings during plant development". Planta. 224 (2). ss. 246-54. doi:10.1007/s00425-005-0205-9. KB1 bakım: Diğerlerinin yanlış kullanımı (link)
- ^ Valderrama; ve diğerleri. (2007). "Nitrosative stress in plants". FEBS Lett. 581 (3). ss. 453-61. doi:10.1016/j.febslet.2007.01.006. KB1 bakım: Diğerlerinin yanlış kullanımı (link)
- ^ Corpas; ve diğerleri. (2004). "Enzymatic sources of nitric oxide in plant cells – beyond one protein–one function". New Phytologist. Cilt 162. ss. 246-7. doi:10.1111/j.1469-8137.2004.01058.x. KB1 bakım: Diğerlerinin yanlış kullanımı (link)
- ^ Judy Siegel-Itzkovich. Viagra makes flowers stand up straight 20 Ağustos 2008 tarihinde Wayback Machine sitesinde arşivlendi.. Student BMJ, September 1999.
- ^ Finer NN, Barrington KJ (2006). "Nitric oxide for respiratory failure in infants born at or near term". Cochrane Database Syst Rev, 4. ss. CD000399. doi:10.1002/14651858.CD000399.pub2. PMID 17054129.
- ^ Chotigeat U, Khorana M, Kanjanapattanakul W (Şubat 2007). "Inhaled nitric oxide in newborns with severe hypoxic respiratory failure". J Med Assoc Thai. 90 (2). ss. 266-71. PMID 17375630. KB1 bakım: Birden fazla ad: yazar listesi (link)
- ^ Hayward C.S., Kelly R.P. and Macdonald P.S. (1999): Inhaled nitric oxide in cardiology practice. Cadio. Vasc. Res. Aug.; 15, 43 (3): 628 - 638.
- ^ Ueber Synthesen stickstoffhaltiger Verbindungen mit Hülfe des Stickoxyds Justus Liebig's Annalen der Chemie Volume 300, Issue 1, Date: 1898, Pages: 81-128 Wilhelm Traube DOI:10.1002/jlac.18983000108
- ^ Nitric Oxide Reacts with Methoxide Frank DeRosa, Larry K. Keefer, and Joseph A. Hrabie J. Org. Chem. 2008, 73, 1139-1142 DOI:10.1021/jo7020423
- ^ Catherine E. Housecroft and Alan G. Sharpe: "Inorganic Chemistry", page 570. Pearson Education Limited 2001, 2005
- ^ Fontijn, A., A. J. Sabadell and R. J. Ronco (1970). "Homogeneous chemiluminescent measurement of nitric oxide with ozone." Analytical Chemistry 42(6): 575-579.
- ^ Vanin A. F.; Huisman A.; van Faassen E.E.; Methods in Enzymology vol 359 (2002) 27 - 42
- ^ Nagano T.; Yoshimura T.; "Bioimaging of nitric oxide", Chemical Reviews vol 102 (2002) 1235 - 1269.
- ^ Kojima H, Nakatsubo N, Kikuchi K, Kawahara S, Kirino Y, Nagoshi H, Hirata Y, Nagano T (1998). "Detection and imaging of nitric oxide with novel fluorescent indicators: diaminofluoresceins". Anal. Chem. 70 (13). ss. 2446-2453. doi:10.1021/ac9801723. PMID 9666719. KB1 bakım: Birden fazla ad: yazar listesi (link)
Konuyla ilgili yayınlar
- Butler A. and Nicholson R.; " Life, death and NO." Cambridge 2003. ISBN 978-0-85404-686-7.
- Corpas FJ et al “Constitutive arginine-dependent nitric oxide synthase activity in different organs of pea seedlings during plant development” Planta 2006 224(2):246-54.
- Corpas FJ, del Río LA, Barroso JB. "Need of biomarkers of nitrosative stress in plants" Trends Plant Sci. 2007 12(10):436-8.
- van Faassen, E. E.; Vanin, A. F. (eds); " Radicals for life: The various forms of Nitric Oxide." Elsevier, Amsterdam 2007. ISBN 978-0-444-52236-8.
- F.A. Cotton, G. Wilkinson, C.A. Murillo, M. Bochmann; Advanced Inorganic Chemistry, 6th ed. Wiley-Interscience, New York, 1999.
- K.J. Gupta, M. Stoimenova, and W. M. Kaiser "In higher plants, only root mitochondria, but not leaf mitochondria reduce nitrite to NO, in vitro and in situ" Journal of Experimental Botany 2005 56(420):2601-2609.
- E. Planchet, K.J. Gupta, M .Sonada & W.M.Kaiser (2005) "Nitric oxide emission from tobacco leaves and cell suspensions: rate limiting factors and evidence for the involvement of mitochondrial electron transport"The Plant Journal 41 (5), 732-743.
- Stöhr, C.; Stremlau, S. "Formation and possible roles of nitric oxide in plant roots" Journal of Experimental Botany 2006 57(3):463-470.
- Pacher, P.; Beckman, J. S.; Liaudet, L.; “Nitric Oxide and Peroxynitrite: in Health and disease” Physiological Reviews 2007, volume 87(1), page 315-424. PMID 17237348.
- Valderrama et al. "Nitrosative stress in plants" FEBS Lett. 2007 581(3):453-61.
Dış bağlantılar
- National Pollutant Inventory - Oxides of nitrogen Fact Sheet
- 1998 Nobel Prize in Physiology/Medicine for discovery of NO's role in cardiovascular regulation 26 Ocak 2002 tarihinde Wayback Machine sitesinde arşivlendi.
- Nitric Oxide and its Role in Diabetes, Wound Healing and Peripheral Neuropathy 22 Haziran 2009 tarihinde Wayback Machine sitesinde arşivlendi.
- Microscale Gas Chemistry: Experiments with Nitrogen Oxides 15 Haziran 2010 tarihinde Wayback Machine sitesinde arşivlendi.
- Your Brain Boots Up Like a Computer 5 Temmuz 2008 tarihinde Wayback Machine sitesinde arşivlendi. - new insights about the biological role of nitric oxide.
- Assessing The Potential of Nitric Oxide in the Diabetic Foot 6 Şubat 2010 tarihinde Wayback Machine sitesinde arşivlendi.
- New Discoveries About Nitric Oxide Can Provide Drugs For Schizophrenia 7 Mayıs 2010 tarihinde Wayback Machine sitesinde arşivlendi.