염화 코발트(II)
| |||
 Structure of anhydrous compound | |||
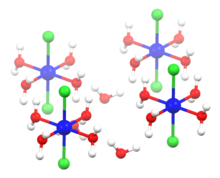 Structure of hexahydrate | |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름 Cobalt(II) chloride | |||
| 별칭 | |||
| 식별자 | |||
| |||
3D 모델 (JSmol) |
| ||
| ChEBI |
| ||
| ChemSpider |
| ||
| ECHA InfoCard | 100.028.718 | ||
| EC 번호 |
| ||
PubChem CID |
| ||
| RTECS 번호 |
| ||
| UNII |
| ||
| UN 번호 | 3288 | ||
CompTox Dashboard (EPA) |
| ||
| |||
SMILES
| |||
| 성질 | |||
| CoCl2 | |||
| 몰 질량 | 129.839 g/mol (anhydrous) 165.87 g/mol (dihydrate) 237.93 g/mol (hexahydrate) | ||
| 겉보기 | blue crystals (anhydrous) violet-blue (dihydrate) rose red crystals (hexahydrate) | ||
| 밀도 | 3.356 g/cm3 (anhydrous) 2.477 g/cm3 (dihydrate) 1.924 g/cm3 (hexahydrate) | ||
| 녹는점 | 726 °C (1,339 °F; 999 K) ±2 (anhydrous)[2] 140 °C (monohydrate) 100 °C (dihydrate) 86 °C (hexahydrate) | ||
| 끓는점 | 1,049 °C (1,920 °F; 1,322 K) | ||
| 43.6 g/100 mL (0 °C) 45 g/100 mL (7 °C) 52.9 g/100 mL (20 °C) 105 g/100 mL (96 °C) | |||
| 용해도 | 38.5 g/100 mL (methanol) 8.6 g/100 mL (acetone) soluble in ethanol, pyridine, glycerol | ||
자화율 (χ) | +12,660·10−6 cm3/mol | ||
| 구조 | |||
| CdCl2 structure | |||
배위 기하 구조 | hexagonal (anhydrous) monoclinic (dihydrate) Octahedral (hexahydrate) | ||
| 위험 | |||
| 물질 안전 보건 자료 | ICSC 0783 | ||
| GHS 그림문자 |    | ||
| NFPA 704 (파이어 다이아몬드) |  0 3 0 | ||
| 인화점 | Non-flammable | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LD50 (median dose) | 80 mg/kg (rat, oral) | ||
| 관련 화합물 | |||
다른 음이온 | Cobalt(II) fluoride Cobalt(II) bromide Cobalt(II) iodide | ||
다른 양이온 | Rhodium(III) chloride Iridium(III) chloride | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.  아니오 확인 (관련 정보 아니오 확인 (관련 정보  예 예 아니오 ?) 아니오 ?) 정보상자 각주 | |||
염화 코발트(II)(Cobalt(II) chloride)는 화학식 CoCl2을 갖는 코발트 및 염소의 무기 화합물이다. 이 화합물은 n = 1, 2, 6, 9가 들어가는 여러 수화물 CoCl
2·nH
2O을 형성한다. 3~4수화물의 형성에 대한 주장은 확증되지 않고 있다.[4] 무수물 형태는 파란 결정 고체이다. 2수화물은 자주색을 보이며 6수화물은 분홍색을 보인다. 상용 샘플들은 보통 6수화물이며 이는 연구실에서 가장 흔히 사용되는 코발트 화합물들 가운데 하나이다.[5]
각주
- ↑ “Cobalt muriate, CAS Number: 7646-79-9”. 《www.chemindustry.com》. 2019년 5월 28일에 원본 문서에서 보존된 문서. 2018년 4월 19일에 확인함.
- ↑ Wojakowska, A., Krzyżak, E. and Plińska, S. (2007): "Melting and high-temperature solid state transitions in cobalt(II) halides". Journal of Thermal Analysis and Calorimetry, volume 88, issue 2, pages 525-530. doi 10.1007/s10973-006-8000-9
- ↑ Santa Cruz Biotechnology: Cobalt(II) chloride
- ↑ M. T. Saugier, M. Noailly, R. Cohen-Adad, F. Paulik, and J. Paulik (1977): "Equilibres solide ⇄ liquide ⇆ vapeur du systeme binaire CoCl
2-H
2O" Journal of Thermal Analysis, volume 11, issue 1, pages 87–100. doi 10.1007/BF02104087 Note: the lowest point of fig.6 is inconsistent with fig.7; probably should be at -27.8 C instead of 0 C. - ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). 《Chemistry of the Elements》 2판. Butterworth-Heinemann. ISBN 978-0-08-037941-8.
외부 링크
- International Chemical Safety Card 0783
- National Pollutant Inventory – Cobalt fact sheet
- IARC Monograph "Cobalt and Cobalt Compounds"
- v
- t
- e
염화물(Cl-)
| HCl(aq) | He | ||||||||||||||||||||
| LiCl | BeCl2 | BCl3 B2Cl4 +BO3 | C2Cl2 C2Cl4 C2Cl6 CCl4 | NCl3 ClN3 | ClxOy Cl2O Cl2O2 ClO ClO2 Cl2O4 Cl2O6 Cl2O7 ClO4 | ClF ClF3 ClF5 | Ne | ||||||||||||||
| NaCl | MgCl2 | AlCl AlCl3 | Si2Cl6 SiCl4 | P2Cl4 PCl3 PCl5 | S2Cl2 SCl2 SCl4 | Cl2 | Ar | ||||||||||||||
| KCl | CaCl CaCl2 | ScCl3 | TiCl2 TiCl3 TiCl4 | VCl2 VCl3 VCl4 VCl5 | CrCl2 CrCl3 CrCl4 | MnCl2 MnCl3 | FeCl2 FeCl3 | CoCl2 CoCl3 | NiCl2 | CuCl CuCl2 | ZnCl2 | GaCl GaCl3 | GeCl2 GeCl4 | AsCl3 AsCl5 | Se2Cl2 SeCl2 SeCl4 | BrCl | Kr | ||||
| RbCl | SrCl2 | YCl3 | ZrCl3 ZrCl4 | NbCl3 NbCl4 NbCl5 | MoCl2 MoCl3 MoCl4 MoCl5 MoCl6 | TcCl3 TcCl4 | RuCl2 RuCl3 RuCl4 | RhCl3 | PdCl2 | AgCl | CdCl2 | InCl InCl2 InCl3 | SnCl2 SnCl4 | SbCl3 SbCl5 | Te3Cl2 TeCl2 TeCl4 | ICl ICl3 | XeCl XeCl2 XeCl4 | ||||
| CsCl | BaCl2 | * | LuCl3 | HfCl4 | TaCl5 | WCl2 WCl3 WCl4 WCl5 WCl6 | ReCl3 ReCl4 ReCl5 ReCl6 | OsCl2 OsCl3 OsCl4 OsCl5 | IrCl2 IrCl3 IrCl4 | PtCl2 PtCl4 | AuCl (Au[AuCl4])2 AuCl3 | Hg2Cl2 HgCl2 | TlCl TlCl3 | PbCl2 PbCl4 | BiCl3 | PoCl2 PoCl4 | AtCl | Rn | |||
| FrCl | RaCl2 | ** | LrCl3 | RfCl4 | DbCl5 | SgO2Cl2 | BhO3Cl | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| * | LaCl3 | CeCl3 | PrCl3 | NdCl2 NdCl3 | PmCl3 | SmCl2 SmCl3 | EuCl2 EuCl3 | GdCl3 | TbCl3 | DyCl2 DyCl3 | HoCl3 | ErCl3 | TmCl2 TmCl3 | YbCl2 YbCl3 | |||||||
| ** | AcCl3 | ThCl4 | PaCl4 PaCl5 | UCl3 UCl4 UCl5 UCl6 | NpCl3 | PuCl3 | AmCl2 AmCl3 | CmCl3 | BkCl3 | CfCl3 | EsCl2 EsCl3 | FmCl2 | MdCl2 | NoCl2 | |||||||







