Kimia organogalium

Kimia organogalium adalah kimia dari senyawa organologam yang mengandung ikatan kimia karbon pada galium (Ga). Meskipun toksisitasnya tinggi,[butuh rujukan] senyawa organogalium memiliki beberapa kegunaan dalam sintesis organik. Senyawa trimetilgalium memiliki beberapa relevansi dengan MOCVD sebagai prekursor galium arsenida melalui reaksinya dengan arsina pada suhu 700 °C:
- Ga(CH3)3 + AsH3 → GaAs + 3CH4
Galium triklorida adalah salah satu reagen penting untuk pengenalan galium ke dalam senyawa organik.
Keadaan oksidasi galium utama adalah Ga(III), seperti pada semua unsur golongan 13 yang lebih rendah (seperti aluminium).[1][2]
Kimia organogalium(III)
Senyawa dengan tipe R3Ga bersifat monomer. Keasaman Lewis menurun dengan urutan Al > Ga > In dan akibatnya senyawa organogalium tidak membentuk dimer penghubung seperti yang dilakukan senyawa organoaluminium. Senyawa organogalium juga kurang reaktif dibandingkan senyawa organoaluminium. Mereka memang membentuk peroksida yang stabil.[3]
Senyawa organogalium dapat disintesis melalui transmetalasi, misalnya reaksi antara logam galium dengan dimetilraksa:
- 2Ga + 3Me2Hg → 2Me3Ga + 3 Hg
atau melalui senyawa organolitium atau Grignard:
- GaCl3 + 3MeMgBr → Me3Ga + 3MgBrCl
Sifat galium yang kekurangan elektron dapat dihilangkan dengan pembentukan kompleks, misalnya
- Me2GaCl + NH3 → [Me2Ga(NH3)Cl]+Cl−
Pembentukan kompleks π dengan alkuna juga dikenal.
Senyawa organogalium adalah pereaksi atau zat antara dalam beberapa kelas reaksi organik:
- Reaksi tipe Barbier dengan galium elemental, substrat alilik, dan senyawa karbonil
- Reaksi karbometalasi (karbogalasi)[4]
Kimia organologam golongan 13 yang lebih tinggi
Kimia organoindium dan kimia organotalium sejajar dengan organogalium dalam banyak hal. Indium dan talium dalam keadaan oksidasi +1 lebih umum, misalnya metalosena siklopentadienilindium(I) dan siklopentadieniltalium. Trimetilindium terbilang penting dalam industri semikonduktor. Ciri khas talium adalah talasi elektrofilik terhadap senyawa arena, yang mirip dengan merkurasi (tetangga golongan 12-nya). Salah satu reagen umum untuk tujuan ini adalah talium(III) trifluoroasetat. Zat perantara ariltalium bisfluoroasetat dapat diisolasi dan diubah menjadi aril halida, aril sianida, aril tiol atau nitroarena. Salah satu contohnya adalah iodinasi para-xilena.[5]
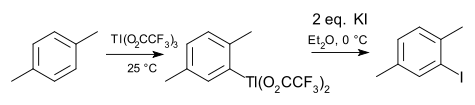 :
:
Topik penelitian indium khusus adalah alilasi yang dimediasi indium.
Referensi
- ^ C. Elschenbroich, A. Salzer Organometallics : A Concise Introduction (Edisi ke-2) (1992) dari Wiley-VCH: Weinheim. ISBN 3-527-28165-7
- ^ Chemistry of aluminium, gallium, indium, and thallium Anthony John Downs (Ed.) ISBN 978-0-7514-0103-5, 1993
- ^ W, Uhl and M. R. Halvagar; et al. (2009). "Reducing Ga-H and Ga-C Bonds in Close Proximity to Oxidizing Peroxo Groups: Conflicting Properties in Single Molecules". Chemistry: A European Journal. 15 (42): 11298–11306. doi:10.1002/chem.200900746. PMID 19780106.
- ^ Amemiya Ryo, Yamaguchi Masahiko (2005). "GaCl3 in Organic Synthesis". Eur. J. Org. Chem. 2005 (24): 5145–5150. doi:10.1002/ejoc.200500512.
- ^ Organic Syntheses, Coll. Vol. 6, hlm.709 (1988); Vol. 55, hlm.70 (1976). Link














