Dithionite de sodium
| Dithionite de sodium | |||
 | |||
 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | Dithionite[1] de sodium | ||
| Synonymes | Hydrosulfite de sodium | ||
| No CAS | 7775-14-6 | ||
| No ECHA | 100.028.991 | ||
| No CE | 231-890-0 | ||
| SMILES | S(S(=O)[O-])(=O)[O-].[Na+].[Na+] PubChem, vue 3D | ||
| InChI | InChI : vue 3D InChI=1/2Na.H2O4S2/c;;1-5(2)6(3)4/h;;(H,1,2)(H,3,4)/q2*+1;/p-2 | ||
| Apparence | Poudre blanche grisâtre | ||
| Propriétés chimiques | |||
| Formule | Na2O4S2Na2S2O4 | ||
| Masse molaire[2] | 174,107 ± 0,011 g/mol Na 26,41 %, O 36,76 %, S 36,83 %, | ||
| Propriétés physiques | |||
| T° fusion | 52 °C (325 K) | ||
| T° ébullition | décomposition au-delà de 100 °C | ||
| Solubilité | 250 g·L-1 (eau, 20 °C) | ||
| Masse volumique | 2,5 g·cm−3 (20 °C) | ||
| Précautions | |||
| SGH[3] | |||
  Danger H251 : Matière auto-échauffante ; peut s'enflammer H302 : Nocif en cas d'ingestion EUH031 : Au contact d'un acide, dégage un gaz toxique | |||
| SIMDUT[4] | |||
  B6, F, B6 : Matière réactive inflammable devient spontanément combustible au contact de la vapeur d'eau F : Matière dangereusement réactive réagit violemment au contact de l'eau en dégageant un gaz très toxique : SO2 Divulgation à 1,0% selon les critères de classification | |||
| NFPA 704 | |||
1 2 2 | |||
| Transport | |||
Code Kemler : 40 : matière solide inflammable ou matière autoréactive ou matière autoéchauffante Numéro ONU : 1384 : DITHIONITE DE SODIUM ; ou HYDROSULFITE DE SODIUM Classe : 4.2 Étiquette :  4.2 : Matières sujettes à l'inflammation spontanée | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
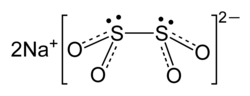
L'hydrosulfite de sodium ou dithionite de sodium Na2S2O4 est une poudre blanche avec une très légère odeur soufrée. Bien qu'il soit stable dans la plupart des conditions, il se décompose dans l'eau chaude ou une solution acide.
Préparation
Le dithionite de sodium peut être obtenu en faisant réagir le bisulfite de sodium avec du zinc selon la formule suivante :
- 2 NaHSO3 + Zn → Na2S2O4 + Zn(OH)2
Utilisation
Il est l'un des agents de blanchiment réducteurs les plus importants. Il est utilisé dans certains procédés de teinture industrielle pour éliminer l'excès de colorant, les oxydes résiduels et les pigments involontaires et pour le blanchiment de la pâte à papier. Il est utilisé aussi comme un réducteur de colorant de cuve. On le retrouve également dans des produits domestiques pour corriger le dégorgement de teintures lors du lavage des vêtements.
Références
- ↑ IUPAC. Nomenclature of Inorganic Chemistry - IUPAC Recommendations 2005, RSC Publishing, 2005, p.329, [lire en ligne]
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ Numéro index 016-028-00-1 dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ « Hydrosulfite de sodium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009
v · m | |
|---|---|
|
 Portail de la chimie
Portail de la chimie













