Methionin
| Methionin | |
|---|---|
 strukturní vzorec | |
| Obecné | |
| Systematický název | (2S)-2-amino-4-(methylsulfanyl)butanová kyselina |
| Triviální název | Methionin |
| Sumární vzorec | C5H11NO2S |
| Identifikace | |
| Registrační číslo CAS | 63-68-3 |
| Vlastnosti | |
| Molární hmotnost | 149,21 g/mol |
| Disociační konstanta pKa | pKCOOH:2,13 pKNH2: 9,28 |
| Izoelektrický bod | 5,74 |
Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). Některá data mohou pocházet z datové položky. | |
Methionin (Met, M) je jedna z dvaceti základních aminokyselin tvořících bílkoviny. Řadí se k nepolárním aminokyselinám a je esenciální (musí být tedy přijímána v potravě).
Funkce methioninu
Methionin je stejně jako všechny ostatní proteinogenní aminokyseliny součástí proteinů (bílkovin). Jeho kodón (kombinace tří bází v mRNA určujících druh aminokyseliny) je AUG, typický start kodon, kterým se začíná syntéza proteinu na ribozomu. Proto je methionin obvykle první aminokyselinou v proteinu, ke které se další aminokyseliny připojují.
Methionin může sloužit pouze pro nastartování tvorby bílkovin a proto je často její počátek s methioninem (formylmethioninem) při posttranslačních modifikacích odštěpen. To je také důvod, proč je methioninu v bílkovinách relativně málo.[1]
Methionin slouží jako donor methylové skupiny. V komplexu S-adenosylmethionin slouží jako koenzym mnoha methylačních enzymů (např. při methylaci bází v DNA nebo methylaci při tvorbě čepičky mRNA).
Methionin se uplatňuje především při tvorbě bílkovin v eukaryotických buňkách. Prokaryota (evolučně velmi staré organismy bez buněčného jádra) používají pro začátek translace modifikovaný methionin - formylmethionin.
Metabolická onemocnění
Odbourávání methioninu je narušeno u následujících metabolických onemocnění:
- homocystinurie
- kombinovaná malonová a methylmalonová acidurie (CMAMMA)
- methylmalonová acidémie
- propionová acidémie
Deriváty
Existuje několik biologicky významných derivátů - aminokyselin odvozených od methioninu:
- formylmethionin - formylovaný methionin, slouží jako první aminokyselina při translaci u prokaryot
- homocystein - demethylovaný methionin (podobá se cysteinu, ale jeho uhlíkový řetězec je o jeden uhlík delší)
-
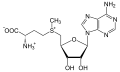 S-adenosylmethionin
S-adenosylmethionin -
 formylmethionin
formylmethionin - homocystein
Reference
- ↑ KODÍČEK, M. methionin. From Biochemické pojmy: výkladový slovník [online]. Praha: VŠCHT Praha, 2007 [cit. 2008-10-13]. Available from:[1]
Externí odkazy
 Obrázky, zvuky či videa k tématu methionin na Wikimedia Commons
Obrázky, zvuky či videa k tématu methionin na Wikimedia Commons
| Proteinogenní aminokyseliny | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Obecná témata | |||||||||||||||||||
| Rozdělení |
| ||||||||||||||||||
| Zvláštní případy | |||||||||||||||||||
| Další rozdělení | |||||||||||||||||||













